Kupfervitriol
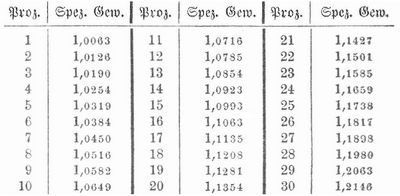
[845] Kupfervitriol (schwefelsaures Kupfer, Kupfersulfat, Kuprisulfat, blauer, cyprischer Vitriol, blauer Galitzenstein, Blaustein) CuSO4 findet sich in der Natur (Chalkanthit) als Zersetzungsprodukt von Kupfererzen, meist in stalaktitischen oder nierenförmigen Aggregaten, als Überzug und Beschlag, auch gelöst in Grubenwassern (Zementwassern), und wird erhalten, indem man Kupferoxyd (Kupferhammerschlag) in verdünnter Schwefelsäure oder metallisches Kupfer in heißer konzentrierter Schwefelsäure löst. Man erhält auch K., wenn man Kupfer mit verdünnter Schwefelsäure bei Luftzutritt behandelt. Zur Darstellung im großen verdampft man Zementwasser zur Kristallisation, oder man röstet Konzentrationsstein (Spurstein), der aus Schwefelkupfer und Schwefeleisen besteht, laugt mit Wasser aus und bringt die Lauge zur Kristallisation. Aus der Mutterlauge, die reich an Eisenvitriol ist, fällt man das Kupfer durch Eisen. Man löst auch geröstetes Schwarzkupfer, Kupferhammerschlag, Malachit (kohlensaures Kupferoxyd) in Schwefelsäure und läßt über Kupfergranalien, Kupferabfälle etc. wiederholt warme verdünnte Schwefelsäure fließen. Beim Affinieren, bei der Silbergewinnung nach Ziervogel und bei der Verarbeitung von Kupferjodür auf Jod entsteht K. als Nebenprodukt. Zur Reinigung von rohem K. kristallisiert man ihn um, nachdem man darin enthaltenen Eisenvitriol durch Erhitzen im Flammofen oxydiert (wobei unlösliches Eisenoxyd entsteht) oder das Eisen durch kohlensaures Kupfer gefällt hat. Über den eisenhaltigen K. des Handels s. Eisenvitriol. K. bildet lasurblaue Kristalle mit 5 Molekülen Kristallwasser, vom spez. Gew. 2,28, besteht in 100 Teilen aus 31,85 Kupferoxyd, 32,07 Schwefelsäure und 36,08 Wasser, schmeckt herb, widerlich metallisch, reagiert sauer, und 100 Teile Wasser lösen bei 10°: 36,9, bei 20°: 42,3, bei 40°: 56,9, bei 80°: 118, bei 100°: 203,3 Teile K. Den Gehalt der Lösungen von verschiedenen spezifischen Gewichten (15°) an kristallisiertem K. zeigt folgende Tabelle:
In Alkohol ist K. unlöslich. Er verwittert in trockner Luft oberflächlich, verliert beim Erhitzen zunächst 4 Moleküle Wasser, wird bei 200° wasserfrei und weiß und zerfällt erst in starker Glühhitze in Kupferoxyd, Sauerstoff und Schweflige Säure. Das weiße wasserfreie Salz ist sehr hygroskopisch und dient zum Entwässern des Alkohols. Man benutzt K. in der Färberei und Zeugdruckerei, zur Darstellung von Kupferfarben, als Fixiermittel für substantive Baumwollfarben (kupfern), in der Galvanoplastik, zum Konservieren des Holzes und der Tierbälge, zum [845] Brünieren des Eisens, zum Färben des Goldes, zum Präparieren der Tonmasse im Deaconschen Chlorbereitungsprozeß, zum Ausbringen des Silbers aus seinen Erzen, zum Beizen des Saatgetreides, in großer Menge und in mehrern Formen (Bordelaiser Brühe etc.) zum Bekämpfen von Pflanzenparasiten, als Brechmittel bei narkotischen Vergiftungen, bei Diphtherie, Phosphorvergiftung, Diabetes, auch äußerlich als Ätzmittel etc. Bei Einwirkung von Kupferoxyd, kohlensaurem Kupferoxyd, ätzenden oder kohlensauren Alkalien auf K. entstehen basische Salze, die sich zum Teil in der Natur in mehreren Mineralien finden, auch in der Farbentechnik benutzt werden. Basisch schwefelsaures Kupfer gibt mit Ammoniak eine tief dunkelblaue Lösung von basisch schwefelsaurem Kupferammoniak, die Baumwolle, Papier etc. zu einer schleimigen Flüssigkeit löst. Mit überschüssigem Ammoniak gibt K. eine tief lasurblaue Lösung, aus der nach vorsichtigem Übergießen mit Alkohol schwefelsaures Kupferoxydammoniak (Kupriammoniumsulfat, Kupfersalmiak) CuSO4+4NH3+H2O kristallisiert. Diese großen, tief dunkelblauen Kristalle riechen schwach ammoniakalisch, schmecken ekelhaft metallisch-ammoniakalisch, lösen sich in 1,5 Teil Wasser, verlieren an der Luft Wasser und Ammoniak und hinterlassen bei 150° die Verbindung CuSO4+2NH3 oder SO4-NH3-NH3-Cu. Man benutzt das Salz in der Feuerwerkerei und als Arzneimittel. K. war schon den Alchimisten bekannt, die oft von eisenhaltigem K. (Verbindung von Venus und Mars) ausgingen, um den Stein der Weisen zu finden. Van Helmont erhielt 1644 K. durch Erhitzen von Kupfer mit Schwefel an der Luft und Glauber 1648 aus Kupfer und Schwefelsäure.
- ZenoServer 4.030.014
- Nutzungsbedingungen
- Datenschutzerklärung
- Impressum