Eisenvitriol
[566] Eisenvitriol (grüner Vitriol, Kupferwasser, grüner Galitzenstein, schwefelsaures Eisenoxydul, Ferrosulfat) FeSO4 findet sich als Zersetzungsprodukt von Schwefelkies in Höhlen und Klüften des Ton- und Kohlenschiefers, in Grubenwässern etc. und entsteht unter Entwickelung von Wasserstoff, wenn man Eisen (Klaviersaitendraht) mit verdünnter Schwefelsäure übergießt. Man erhitzt die grüne Lösung zuletzt mit überschüssigem Eisen zum Sieden, filtriert sie noch heiß in eine mit Schwefelsäure ausgespülte Flasche und läßt kristallisieren. Die Kristalle werden gut abgespült und bei 30° getrocknet. Filtriert man die Lösung in starken Alkohol, so entstehen bläulichweiße, kleine Kristalle, die, mit Weingeist abgewaschen und getrocknet, selbst an feuchter Luft sich nur langsam verändern. Sehr reinen E. gewinnt man als Nebenprodukt bei der Bereitung von Schwefelwasserstoff aus Schwefeleisen. In der Technik läßt man Schwefelkiese (Zweifachschwefeleisen) an der Luft verwittern und bringt in die Lösung, die C. und freie Schwefelsäure enthält, Eisenabfälle, um die freie Schwefelsäure zu neutralisieren, und um aus dem C. stets sich bildendes schwefelsaures Eisenoxyd zu E. zu reduzieren. Enthalten die Erze Tonerdeverbindungen, so bildet die freie Schwefelsäure schwefelsaure Tonerde. Diese wird auf Alaun verarbeitet, und es hängt ganz von dem Verhältnis ab, in dem sich in den Erzen Schwefelkies und Tonerde finden, ob man aus der Lauge zuerst Alaun und nur aus der Mutterlauge E. oder umgekehrt zuerst E. und aus der Mutterlauge Alaun gewinnt. Bisweilen werden die Alaunerze zunächst geröstet und geben dann beim Auslaugen eine Lösung von E. und schwefelsaurer Tonerde, auch destilliert man aus Schwefelkiesen Schwefel ab und läßt die entschwefelten Kiese verwittern. E. wird auch durch Kohlen von gepochten Eisenfrisch- und Puddelschlacken oder Spateisenstein (kohlensaurem Eisenoxydul) mit Schwefelsäure, aus Eisenabfällen und Kammersäure oder aus Schwefelsäure dargestellt, die zur Reinigung von Rohpetroleum, Mineralölen oder zur Darstellung von Nitrobenzol etc. gedient hat; Eisenwarenfabriken, die Schwefelsäure zum Abbeizen[566] brauchen, wie Drahtziehereien etc., stellen wohl E. dar, weil sie die Säure nicht ungesättigt abfließen lassen dürfen. Auch bei Verarbeitung von Kupfererzen auf nassem Wege wird E. gewonnen. Die verdampfte Lösung von E. wird zur Kristallisation in Gefäße gebracht, die mit Strohhalmen oder Holzstäben versehen sind. An diesen setzen sich dann die Kristalle als Traubenvitriol ab. Die am Boden und an den Wandungen minder schön ausgebildeten Kristalle bilden die Tafeln. Durch verschiedene Metallsalze verunreinigt ist der fast dunkelbraune Schwarzvitriol, der zuweilen auf den Hütten nachgeahmt wird, indem man grünen E. durch einen Ausguß von Erlenblättern oder Galläpfeln schwarz färbt. Aus kupferhaltigen Kiesen entsteht durch Verwitterung auch Kupfervitriol, der mit dem E. in wechselnden Mengen zusammenkristallisiert. Kupferhaltiger E. (Salzburger oder Admonter, Bayreuther, Gräfenthaler Doppelvitriol, Adlervitriol) wurde für manche Zwecke in der Färberei benutzt, wird aber vorteilhafter durch Mischungen von reinem Eisen- und Kupfervitriol ersetzt. In manchen Bergwerken entstehen durch Oxydation von Schwefelkies Grubenwasser, aus denen, wenn sie auch Kupfervitriol enthalten (Zementwasser), zunächst durch Einlegen von Eisen metallisches Kupfer abgeschieden wird. Diesem Umstand verdankt der E. seinen ältern Namen Kupferwasser.
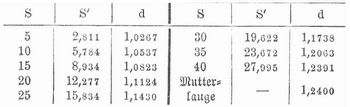
E. bildet blaugrüne Kristalle mit 7 Molekülen Kristallwasser und besteht aus 26,1 Teilen Eisenoxydul, 29,9 Teilen Schwefelsäure und 44 Teilen Wasser. Er besitzt das spez. Gew. 1,89, schmeckt zusammenziehend tintenartig, verwittert leicht an der Luft und zerfällt unter Oxydation zu gelblichem basisch schwefelsauren Eisenoxyd. Eisenoxydhaltiger E. ist grün, wird an der Luft feucht und oxydiert sich schneller als der reine E. Auch die Lösung oxydiert sich an der Luft schnell. 100 Teile Wasser lösen bei
In der folgenden Tabelle bedeutet S den Prozentgehalt einer Lösung an kristallisiertem E., S´ den Gehalt an wasserfreiem Salz und d das spezifische Gewicht der Lösung bei 15°.
In Alkohol ist E. unlöslich. Beim Erhitzen schmilzt er und hinterläßt bei 100° ein Salz mit 1 Molekül Kristallwasser, das bei stärkerm Erhitzen farblosen wasserfreien E. hinterläßt, der in noch höherer Temperatur in schweflige Säure und basisch schwefelsaures Eisenoxyd zerfällt; letzteres gibt endlich Eisenoxyd und Schwefelsäureanhydrid. Bei 80° kristallisiert E. mit 4 Molekülen Wasser. Die wässerige Lösung von E. absorbiert Stickoxydgas unter dunkelbrauner Färbung. Es wirkt stark reduzierend. Schwefelsaures Eisenoxydulammoniak (Ammoniumferrosulfat, Eisensalz, Mohrsches Salz) FeSO4(NH4)2SO4 + 6H2O wird erhalten durch Vermischen konzentrierter Lösungen von E. und schwefelsaurem Ammoniak; es bildet bläuliche Kristalle vom spez. Gew. 1,81 und ist sehr viel beständiger als E. 100 g Wasser lösen bei 0° 12, bei 75° 57 g wasserfreies Salz. Man benutzt E. als Desinfektionsmittel, in der Färberei zum Schwarzfärben (mit Gerbsäure) und zum Blaufärben (mit Blutlaugensalz), beim Gerben mit Eisensalzen, zur Bereitung von Tinte und Lederschwärze, zur Bereitung von Berlinerblau, zur Darstellung von rauchender Schwefelsäure, zum Fällen des Goldes und Silbers aus ihren Lösungen, zum Gewinnen von Kupfer auf nassem Wege, zur Herstellung von Indigoküpe, zur Reduktion von Nitroverbindungen, zur Vertilgung des Hederich und als Arzneimittel. Das schwefelsaure Eisenoxydulammoniak wird in der Photographie und in der Maßanalyse benutzt. – E. war höchstwahrscheinlich, wenn auch nur in unreinem Zustand, schon den Alten bekannt. Das Atramentum sutorium (»Schusterschwärze«) der Römer war wohl größtenteils E., es wurde aber nicht vom Kupfervitriol unterschieden. Man benutzte es als Heilmittel und zum Schwärzen des Leders. Albertus Magnus erwähnt zuerst im 13. Jahrh. den E. mit Bestimmtheit, und Basilius Valentinus lehrte im 15. Jahrh. seine Darstellung aus Schwefelkies sowie aus metallischem Eisen und Schwefelsäure. Agricola sprach von der Verwitterung der Kiese, und Vigani beschrieb 1683 die Fällung des Kupfers aus Vitriollauge durch Einlegen von Eisen.
- ZenoServer 4.030.014
- Nutzungsbedingungen
- Datenschutzerklärung
- Impressum